LC-Q-Orbitrap HRMS를 사용한 대사체 프로파일링
일반적으로 대사체학 연구에서는 샐비어 음이온화 모드의 종은 양성 모드의 종보다 더 효율적인 경향이 있습니다.15. 본 연구에서 MS 데이터 분석에는Compound Discoverer 2.1 소프트웨어에서 제공하는 온라인 및 로컬 데이터베이스의 사용이 포함되었습니다. 또한, 이전 대사체학 연구에서 수집된 데이터는 다음과 같습니다. 샐비어 종은 수집되어 대량 목록으로 병합되어 로컬 데이터베이스로 구현되었습니다. 총 2704개의 물질 피크가 검출되었습니다. S. 프루티코사 음이온 모드 분석에서 추출합니다. 사소한 신호를 필터링한 후(Area < 104), 보충표에 나타난 바와 같이 95개의 대사산물이 잠정적으로 식별된 98개의 대사산물이 있었습니다. S1.
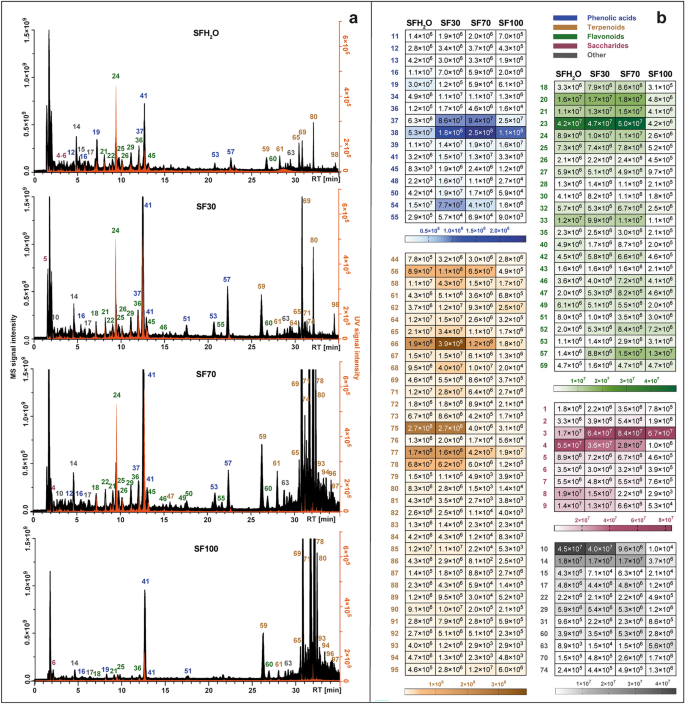
각 추출물의 대사산물 프로파일을 병치하여 그림 1에 나타내었습니다. 1ㅏ. 지배적인 그룹은 다른 추출물들 사이에서 변화했습니다. 대부분 물을 함유한 용매(SFH)로 얻은 것2O 및 SF30) 가장 풍부한 화합물은 페놀산이었습니다. 테르페노이드 화합물의 추출 효율은 이들 화합물의 비극성 특성으로 인해 사용된 용매에서 에탄올의 증가와 일치했습니다. 또한, 네 가지 다른 식물에서 검출된 개별 식물화학물질의 신호 강도를 보여주는 히트맵이 제공됩니다. S. 프루티코사 추출물은 그림 1에 나와 있습니다. 1비. 연구된 추출물에서 검출된 가장 많은 종류의 화합물은 35개 화합물이 포함된 테르페노이드였으며, 플라보노이드(24개 화합물), 페놀산 및 유도체(19개 화합물), 당류(9개 화합물) 및 기타 지방산, 카르복실산 및 미확인 화합물이 그 뒤를 이었습니다. .
270 nm(주황색)에서 UV-Vis 검출기에 의해 등록된 크로마토그램과 결합된 음성 모드(검은색)의 LC-Q-Orbitrap에서 얻은 총 이온 크로마토그램(ㅏ), 확인된 화합물의 평균 MS 피크 면적 값을 나타내는 히트 맵으로 설정 S. 프루티코사 추출물 : SFH2O-물 추출물; SF30-30% 에탄올 추출물; SF70-70% 에탄올 추출물; SF100–에탄올추출물(비). 피크의 식별은 보충 표를 참조하십시오. S1.
가장 극성이 높은 두 가지 추출물(SFH)의 경우2O 및 SF30) 페놀산은 전체 피크 면적에서 가장 풍부한 종류였습니다. 이 클래스는 주로 카페인산 유도체로 대표됩니다. 화합물의 체류 시간(RT) 16 전구체 이온 [MH]̅ m/z 179.03419는 카페인산 표준의 RT와 일치했습니다. 또한 다음에서 특징적인 주요 조각을 생성했습니다. m/z 135.04414, 이산화탄소 손실로 인해. 카페인산의 양성자가 제거된 형태가 화합물에서 검출되었습니다. 40 그리고 41, 이는 사게린산([MH]̅)으로 확인되었습니다. m/z 719.16210) 및 로즈마린산([MH]̅ at m/z 359.0773). 표준품과의 비교를 통해 로즈마린산 동정을 추가로 확인하였습니다. 화합물에 대해서도 동일한 이온 또는 그 손실이 관찰되었습니다. 20, 37, 39, 44, 53, 57 그리고 58, 문헌 및 MS와의 비교를 통해 뒷받침됨2 단편화는 살비아플라사이드([MH]̅)로 확인되었습니다. m/z 521.13012), 살비아놀산 B([MH]̅ at m/z 717.14661), 이소살비아놀산 B([MH]̅ at m/z 717.14667), 살비아놀산 K([MH]̅ at m/z 555.11469), 두 개의 살비아놀산 F 이성질체([MH]̅ at m/z 313.07205) 및 살비아놀산 C([MH]̅ at m/z 491.09863).
가장 비극성인 두 가지 추출물(SF70, SF100)의 경우 테르페노이드의 기여도가 가장 높았고 나머지 추출물에서는 이 클래스가 확인된 화합물의 피크 면적 합계의 약 4분의 1을 차지했습니다. 이 클래스는 연구된 추출물에서 확인된 가장 다양한 비극성 클래스의 화합물인 디테르페노이드로 주로 대표되었습니다. 그들은 대부분 아비에탄형 디테르페노이드였으며, 음이온화를 통한 단편화에는 종종 CO 제거가 포함되었습니다.2 (-44 Da), CO (-28 Da), H2O(-18 Da), ·CH3 (15다). 화합물 59 ([MH]̅ 에 m/z 345.17075) 및 64 ([MH]̅ 에 m/z 345.17100) 둘 다 이산화탄소 분자의 손실로 인한 이온을 나타냈습니다(m/z 301.18097) 및 물 분자(m/z 283.17038 및 m/z 283.17041), 로스마놀 및 에피이소로스마놀로 확인되었습니다. 화합물 69 ([MH]̅ 에 m/z 329.17580)은 이산화탄소 손실로 시작하는 전형적인 단편화 패턴을 기반으로 카르노솔로 식별되었습니다(m/z 285.16604)12,15 이어서 메틸 라디칼이 제거됩니다(m/z 270.16211). 복합에서도 동일한 조각화 패턴이 발생했습니다. 80, 12-메톡시 카르노산([MH]̅)으로 확인되었습니다. m/z 345.20721) 301.21689 및 286.19385의 단편이 포함되어 있습니다. 화합물 78, 유사분자 이온과 함께 m/z 331.19153 [MH]̅는 이산화탄소 손실과 그에 따른 이소프로필 라디칼의 손실에 해당하는 조각이 존재하기 때문에 카르노산으로 식별되었습니다(m/z 287.20175 및 244.14687). 화합물 70 [MH]̅에서 전구체 이온을 나타냈습니다. m/z 343.15524, 특징적인 조각을 생성함 m/z 315.16028 및 m/z 299.160504 각각 에틸렌과 이산화탄소의 손실을 통해 발생합니다. 이를 통해 화합물을 식별할 수 있습니다. 70 로즈마디알처럼. 두 가지 오환식 트리테르페노이드도 테스트된 추출물에서 검출되었습니다. 96 그리고 97, 이는 잠정적으로 각각 베툴린산과 우르솔산으로 확인되었으며, ([MH]̅ 에 준분자 이온이 있음) m/z 455.35340). 이러한 트리테르페노이드의 존재는 다음에서도 보고되었습니다. S. 프루티코사 Jash et al.16.
연구된 추출물, 특히 수분 함량이 높은 추출물(SFH)에서2O, SF30), 확인된 화합물의 전체 피크 면적에서 올리고당과 당산의 상당 부분도 주목되었습니다. 화합물 1, 2 그리고 3 잠정적으로 스타키오스(stachyose), 라피노스(raffinose), 수크로스(sucrose)로 확인되었는데, 이는 종종 체내에서 주요 수송당이기 때문입니다. 샐비어 종31. 화합물 4~8 당산으로 분류되었습니다. 화합물의 단편화 패턴 6 ([MH]̅ 에 m/z 135.02875)와 동일합니다. 엘-트레온산. 화합물 8 ([MH]̅ 에 m/z 149.0081) 생성된 조각 m/z 72.99171, 59.01249 및 87.00734는 음이온화 모드에서 관찰할 수 있습니다. 엘-( +)-타르타르산.
또 다른 주요 종류의 식물화학물질이 발견되었습니다. S. 프루티코사 추출물은 플라보노이드였습니다. 이 클래스에 속하는 확인된 화합물의 대부분은 플라본에 할당되었습니다. 화합물 24 머무름 시간, UV 스펙트럼 및 MS/MS 단편화 패턴을 상용 표준과 비교하여 scutellarin으로 명확하게 식별되었습니다. 화합물 46 그리고 55 에서 거의 동일한 전구체 이온 [MH]̅을 나타냈습니다. m/z 299.0563 및 299.0562. 화합물 46 가장 많은 조각을 생성했습니다. m/z 284.03253 및 136.98682, 유사 화합물 55. 이 데이터는 히피둘린 또는 디오스메틴의 단편화 패턴과 일치합니다. 머무름 시간에 차이가 있었기 때문에 두 화합물 모두에 존재할 수 있었습니다. S. 프루티코사 추출물. 화합물 49 [MH]̅에서 전구체 이온을 나타냈습니다. m/z 285.04065는 특정 생성물 이온을 형성했습니다. m/z 133.02834, 151.00261, 175.03903, Velamuri 등이 루테올린에 대해 보고한 내용과 일치합니다.17. 화합물 52 ([MH]̅ 에 m/z 327.21786)은 이전에 보고된 바와 같이 salvigenin(pectolinarigenin-7-methyl ether)으로 확인되었습니다. S. 프루티코사. 화합물 54 에서 기본 피크 [MH]̅를 산출했습니다. m/z 269.04578. 전구체 이온 및 생성 이온 m/z 117.03332 및 151.00264에서는 이 화합물이 아피게닌임을 확인하였다. 화합물 56 전구체 이온 [MH]̅를 다음과 같이 제공했습니다. m/z 329.0668, 이는 분자식이 C임을 나타냅니다.17시간14영형7. 그것은 눈에 띄는 조각 이온을 생성했습니다. m/z 299.01981은 2개의 메틸기의 손실에 기인하고, 271.02472는 일산화탄소의 추가적인 제거에 기인합니다. 따라서 이 피크는 jaceosidin으로 확인되었다. 화합물 60 에서 전구체 이온 [MH]̅에 기초하여 cisimaritin으로 확인되었습니다. m/z 313.07190 및 진단 생성물 이온 m/z 298.04694 및 283.02478은 두 개의 메틸 라디칼의 손실을 나타내며 일산화탄소 제거로 인한 255.02974입니다. 화합물 62 ([MH]̅ 에 m/z 283.06137)은 다음의 단편을 고려한 아피게닌 유도체에 해당합니다. m/z 268.03772 및 117.03318. 특징적인 단편 이온 m/z 240.04193 일산화탄소의 손실로 인해 형성된 화합물 62 genkwanin으로 식별됩니다. apigenin, hispidulin, cirsimaritin 및 genkwanin의 단편화 패턴은 Koutsoulas et al.12. 화합물 50 연구된 추출물에서 검출된 유일한 유형의 플라보놀 아글리콘이었습니다. 전구체 이온 [MH]̅ m/z 315.0513 및 주요 MS/MS 단편 m/z 메틸 그룹이 손실된 300.02756 이 화합물은 isorhamnetin으로 확인되었습니다. 화합물 30 유사분자 이온 [MH]̅ 에 m/z 609.18329는 조각화를 나타내지 않았지만 이전에 보고되었기 때문에 S. 프루티코사18,19, 그것은 플라바논(flavanone)-헤스페리딘(hesperidin)으로 잠정적으로 확인되었다. 본 연구에서 발견된 플라보노이드 배당체는 주로 162 Da의 특징적인 단편을 갖는 글루코사이드, 글루쿠로니드(176 Da) 및 루티노사이드(308 Da)였습니다. 루테올린 글루코사이드(화합물) 22 [MH]̅ 와 함께 m/z 447.09344)는 다음의 화학적 조성에 관한 대부분의 간행물에 존재합니다. S. 프루티코사 추출물12,18,19,20,21. 화합물 26 전구체 이온 [MH]̅을 보여주었다. m/z 491.0836이며 이전에 보고된 isorhamnetin glucuronide로 확인되었습니다. S. 프루티코사 Gürbüz et al.22. 화합물 27 ([MH] ́ m/z 577.15668), apigenin-rutinoside로 확인된 것은 Cvetkovikj et al.에 의해 그리스 세이지에서도 발견되었습니다.21.
지방산의 존재도 관찰되었습니다. S. 프루티코사 추출물. 화합물 63 그리고 73 두 개의 다중불포화지방산으로 잠정적으로 확인되었습니다. 화합물 63 dihydroxyoctadecadienoic acid(C)로 지정되었습니다.18시간31영형4̅). 화합물 73 생성된 전구체 이온 [MH]́ m/z 295.22803 및 특성 조각 중/지 277.21738 ([MHH2영형]- 및 195.13837 [M-(CHO-(CH2)4-CH3)-H]̅는 13개의 탄소 원자에서 수산기의 위치를 나타냅니다. 따라서 이는 13-hydroxy-9,11-octadecadienoic acid로 확인되었습니다. 또한 에서는 S. 프루티코사 투베론산의 글루코사이드 존재를 추출합니다(m/z 387.16644) (복합 14) 성장호르몬인 것이 관찰되었다.
주요 식물화학물질의 정량분석
다양한 추출물의 주요 페놀성 화합물 정량화 S. 프루티코사 식물 재료의 건조 중량(mg/g DW)이 표에 나와 있습니다. 1. 카페산, 스쿠텔라린, 살비아놀산 B, 로즈마린산, 카르노식산 및 카르노솔의 함량은 실제 표준의 검량선을 기반으로 계산되었으며, 다른 화합물의 함량은 가장 유사한 사용 가능한 표준을 기준으로 추정되었습니다.
전반적으로, 세이지 추출물에 가장 풍부한 화합물은 로즈마린산으로, 이는 페놀산이자 카페인산의 이량체입니다. 모든 테스트 샘플 중 로즈마린산 농도가 가장 높은 것은 SF70(31.56 ± 1.88 mg/g DW)에서 발견되었으며, 이는 S. 프루티코사 Mervić et al.에 의해 보고된 크로아티아(29.10 ± 0.21 mg/g DW)에서 수집되었습니다.23. Sarrou 등이 연구한 그리스 다양한 세이지의 메탄올 추출물에서는 훨씬 더 높은 함량(60.73 mg/g DW)이 보고되었습니다.19그러나 본 연구에서는 순수 알코올을 용매로 사용한 결과 로즈마린산의 최고 수율이 나오지 않았습니다. 주입 시 로즈마린산 농도(SFH)2O)는 다른 추출물보다 훨씬 낮았습니다(4.96 ± 0.65 mg/g DW). 이는 터키 품종에 대한 유사한 비교 결과와 일치하지 않습니다. S. 프루티코사 작성자: 테킨18. 카페인산은 연구된 모든 추출물에서도 비슷한 농도(0.13~0.15 mg/g DW)로 검출되었는데, 이는 Mervić 등이 보고한 것보다 10배 더 낮았습니다.23. 그러나 세이지 식물의 주요 카페산 유래 삼량체에 속하는 살비아놀산은 거의 더 많은 양으로 존재하지 않았습니다. SF70 및 SF30 추출물에서 가장 높은 농도의 살비아놀산 B가 얻어졌습니다(6.86 ± 0.93 mg/g DW 및 6.52 ± 0.48 mg/g DW). Salvianolic acid K는 6.25 ± 1.0 mg/g DW의 농도로 ST30 추출물에서 가장 풍부했습니다. Cvetkovikj et al.이 제시한 데이터에 따르면.21, 연구된 여러 그리스 인구 중 살비아놀산 K의 최대 농도 S. 프루티코사 7.20 mg/g DW였습니다.
가장 풍부한 테르페노이드 화합물 S. 프루티코사 카르노산과 카르노솔은 둘 다 아비에탄 디테르페노이드 계열에 속합니다.12. 카르노식산 함량은 SF100(14.82 ± 1.66 mg/g DW)에서 가장 높았고 SF70(13.88 ± 2.52 mg/g DW)이 그 뒤를 이었습니다. 이는 통계적으로 차이가 없습니다. 이러한 결과는 Kallimanis et al.이 메탄올 추출물에서 측정한 함량과 일치합니다.24 이는 12.5 ± 1.6 mg/g DW였습니다. SF70 추출물의 카르노솔 양은 7.88 ± 1.33 mg/g DW였으며 이는 Sarrou 등이 보고한 것과 일치했습니다.19. 연구된 추출물에서 세 번째로 풍부한 테르페노이드인 살비올은 아비에탄 디테르페노이드(페루지놀)에서 파생된 메로테르페노이드이며 다른 그리스 종의 세이지에서 흔히 발견됩니다. S. 포미페라25. 이 화합물은 아직 보고되지 않았습니다. S. 프루티코사; 그러나 이는 SF70에서 7.37 ± 0.71 mg/g DW로 가장 높은 함량으로 연구된 대부분의 추출물에 존재했습니다.
세 번째 그룹의 생리활성물질이 검출되었습니다. S. 프루티코사 추출물은 플라보노이드였습니다. 스쿠텔라린은 세이지에서 발견되는 일반적인 플라보노이드 중 하나입니다.26. 유사한 수율로 연구된 추출물에서 가장 풍부한 플라보노이드였습니다: SFH에서 7.77 ± 0.48 mg/g DW, 8.92 ± 1.56 mg/g DW 및 7.35 ± 0.9 mg/g DW2O, SF30 및 SF70 추출물. 루테올린 루티노사이드와 루테올린 글루코사이드의 농도는 연구된 모든 추출물에서 유사했고 범위는 1.03~1.98 mg/g DW였으며, 이는 Tekin 등이 보고한 데이터와 일치하지 않습니다.18샐비어 차에 함유된 이들 화합물의 농도는 에탄올 추출물에 비해 2~3배 더 높았습니다.
페놀산, 플라보노이드 및 테르페노이드가 대표적인 생리 활성 화합물입니다. S. 프루티코사. 표에 표시된 바와 같이 1, 추출 수율은 용매의 에탄올 함량에 따라 크게 영향을 받습니다. 70% 에탄올을 이용한 추출은 물로만 추출한 것에 비해 가장 높은 총 생리활성물질 수율을 제공했습니다. 그 차이는 페놀산과 테르페노이드의 수율에서 명확히 드러납니다. SF70에서는 각각 3배, 7배 더 높았습니다. 플라보노이드의 최대 추출 수율은 30% 에탄올에서 얻어졌으나 70% 에탄올에서 얻은 것보다 약간 높았을 뿐이다. 연구된 생리활성물질의 모든 그룹을 고려할 때, 70% 에탄올은 생리활성 화합물 추출을 위해 테스트된 용매 중에서 가장 좋은 용매인 것으로 결론지었습니다. S. 프루티코사.
항산화 활성
식물 재료에서 항산화 활성을 나타내는 화합물의 존재는 건강 증진 특성을 정의하는 중요한 측면이 되었습니다. 다양한 종류의 세이지의 경우 높은 항산화 활성은 주로 페놀성 화합물에 의해 발생합니다. 제시된 연구에서 총 항산화 활성은 다음과 같이 결정되었습니다. S. 프루티코사 서로 다른 극성의 추출제로 제조된 추출물. 또한, 세이지에 전형적이고 페놀산, 플라본 및 디테르페노이드와 같은 다양한 종류의 2차 대사산물에 속하는 선택된 페놀성 화합물에 대한 항산화 활성이 측정되었습니다.
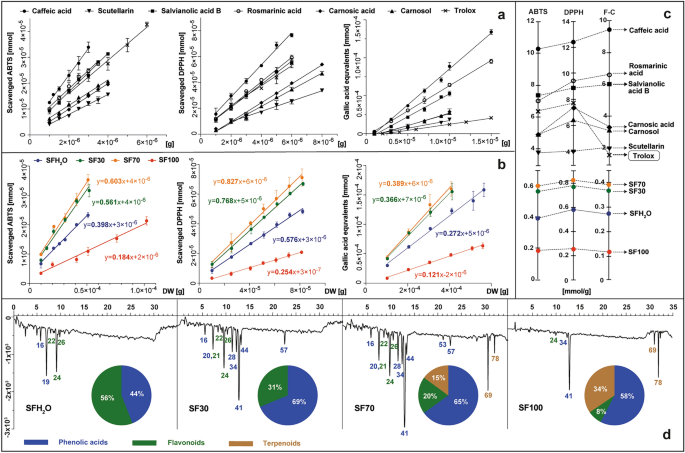
제시된 연구에서는 ABTS, DPPH 및 Folin-Ciocalteu(F-C) 시약을 사용하여 가장 널리 사용되는 세 가지 분광 광도계 테스트 결과를 비교했습니다. ABTS 및 DPPH 분석은 순수 화합물과 마찬가지로 추출물의 자유 라디칼 소거 활성을 결정하는 데 널리 사용됩니다. 을 위한 S. 프루티코사 추출물에서 계산된 항산화 활성은 10분 반응 후 건조 물질 1g에서 유래된 항산화제에 의해 감소된 ABTS 또는 DPPH 분자의 수를 나타냅니다. 이 값은 방법의 선형 범위에서 계산되었으며 산화제의 감소된 밀리몰 수와 다양한 양의 테스트 샘플(반응 혼합물의 건조 물질 그램) 사이의 관계를 설명하는 선의 기울기로 표현되었습니다(그림 1). 2비).
표준품(카페산, 스쿠텔라린, 살비아놀산 B, 로즈마린산, 카르노식산, 카르노솔 및 트롤록스)의 항산화 활성 S. 프루티코사 추출물 : SFH2O-물 추출물; SF30-30% 에탄올 추출물; SF70-70% 에탄올 추출물; ABTS, DPPH 및 F-C 시약을 사용하여 시험관 내에서 테스트한 SF100-에탄올 추출물은 테스트된 표준에 따라 감소된 시약의 의존성 곡선을 보여주는 플롯으로 표시됩니다(ㅏ) 또는 추출(비) 그리고 테스트 샘플 1g으로 감소된 시약의 밀몰몰과 동일한 곡선의 기울기로 표현됩니다(씨)는 ABTS를 사용한 컬럼 후 유도체화 후 734 nm에 등록된 추출물의 항산화 프로파일로 설정되었으며 원형 차트에는 주요 항산화 물질 클래스가 표시되어 있습니다(디). 피크의 식별은 보충 표를 참조하십시오. S1.
이 연구에는 Folin-Ciocalteu 시약을 사용한 방법도 포함됩니다. 이는 활성 수산기를 갖는 화합물에서 인몰리브덴 인텅스텐산 복합체로 알칼리성 환경에서 전자를 전달하는 것으로 구성됩니다. 이 경우 환원 능력은 청색 복합체를 형성하고 식물의 건조 물질 1g에서 파생된 갈산 당량의 밀리몰 수로 표현되었습니다. 카페인산, 카르노식산, 카르노솔, 살비아놀산 B, 스쿠텔라린, 로즈마린산 및 추가로 참조 항산화제인 트롤록스와 같은 세이지에 존재하는 선택된 순수 물질에 대해 동일한 접근법이 사용되었습니다(그림 1). 2ㅏ). 식물 재료와 순수 물질의 항산화 활성을 측정하고 계산하는 방법은 이전에 Kusznierewicz et al.에 의해 설명되었습니다.27 및 Baranowskaet al.28, 각각. 결과 기울기 값은 표준 및 샘플에 대해 수행된 각 테스트에 대해 별도의 축에 표시되었습니다(그림 1). 2씨). 테스트된 각 페놀성 표준물질은 항산화 활성을 나타냈으며, 스쿠텔라린 < 카르노솔 < 카르노산 < 살비아놀산 B < 로즈마린산 < 카페산 순으로 증가했습니다. 그 중 3개(살비아놀산 B, 로즈마린산, 카페인산)는 항산화 활성 측정 분석에서 일반적으로 참고 자료로 사용되는 화합물인 트롤록스보다 더 효율적이었습니다. 연구된 모든 추출물의 항산화 활성 S. 프루티코사 DPPH 테스트뿐만 아니라 ABTS 분석에서도 용량 의존적이었습니다. 따라서 반응 혼합물에 첨가된 추출물의 양이 증가함에 따라 이러한 라디칼에 대한 환원력도 증가합니다. SF100 추출물의 총 항산화 활성이 가장 낮았고 SFH의 경우 거의 2배 더 높았습니다.2O, SF30 및 SF70의 경우 거의 4배 더 높습니다. F-C 테스트 결과는 ABTS 및 DPPH와 동일한 경향을 보였으며 Pearson 상관관계는 0.99였습니다. 이는 Lantzouraki 등이 입증한 것처럼 추출물의 항산화 활성이 페놀 함량에 크게 좌우된다는 것을 나타냅니다.29.
시험을 위해 선정된 6가지 파이토케미컬 추출물의 함량을 기준으로 합니다. (표 1) 및 이들과 추출물에 대해 결정된 항산화 활성(그림 1). 2a,c), 우리는 개별 추출물의 총 항산화 활성에 대한 이들 화합물의 추정 기여도를 결정할 수 있습니다. SFH의 경우2O, SF30 및 SF70 추출물, 6가지 선택된 화합물은 테스트에 따라 이론적으로 각각 결정된 총 항산화 활성의 21-30%, 45-63% 및 64-86%를 포괄했습니다. 이러한 결과는 이들 추출물 및/또는 이들의 시너지 효과에 다른 추가 항산화제가 존재할 가능성이 있음을 시사합니다. SF100 추출물의 경우에만 6가지 표준 화합물의 활성 합계가 사용된 테스트에 따라 20~49% 범위에서 이 추출물의 결정된 총 활성을 초과했습니다. 이러한 관찰은 이러한 종류의 추출물에 존재하는 식물화학물질 간의 가능한 길항적 상호작용의 결과일 수 있습니다.
테스트에 존재하는 항산화제 유형에 대한 자세한 정보 S. 프루티코사 ABTS 시약을 사용한 HPLC 컬럼 후 유도체화를 사용하여 추출물을 제공했습니다. 이 방법으로 얻은 항산화 프로파일과 총 항산화 활성에서 다양한 종류의 항산화제의 기여도가 그림 1에 나와 있습니다. 2디. 앞서 테스트한 6가지 표준 항산화제 외에도 S. 프루티코사 추출물에는 프르제발스킨산 A, 살비아플라사이드, 루테올린 루티노사이드, 루테올린 글루코사이드, 이소르함네틴 글루쿠로니드, 쿠마로일 카페오일글리코사이드, 살비아놀산 K 및 살비아놀산 F와 같은 다른 항산화제도 포함되어 있습니다. SF70 및 SF30 추출물에서 ABTS 라디칼이 관찰되었습니다. 이 두 샘플의 항산화 프로필의 유사성에도 불구하고 공통 신호의 강도는 SF70에서 더 높았으며 디테르페노이드에서 유래한 추가 활성도 나타났습니다. SF70 및 SF100 추출물의 프로필에서만 디테르페노이드에서 유래한 음성 피크가 관찰되었으며, 이는 각각 15 및 34%에서 총 항라디칼 활성을 공유합니다. 에탄올을 함유한 모든 추출물의 주요 항산화제는 로즈마린산이었습니다. 이는 가장 풍부한 페놀산이자 연구된 표준 중에서 가장 강력한 항산화제 중 하나입니다. 에 대해서도 동일한 결과가 보고되었습니다. S. 오피시날리스 그리고 S. 히스파니카 추출물30,31.
수성추출물(SFH2O) 항산화 활성은 주로 przewalskinic acid A와 scutellarin의 두 가지 화합물에서 유래했는데, 이는 로즈마린산을 물만으로 추출하는 경우 효과가 덜했기 때문입니다.
잔틴산화효소 저해활성
잔틴 산화효소(XO)는 하이포잔틴과 잔틴이 요산으로 산화되는 것을 촉매합니다. 요산이 혈액에 과도하게 존재하면 통풍이 발생합니다. XO 재산화 동안 분자 산소는 전자 수용체 역할을 하여 과산화물 라디칼과 과산화수소를 생성합니다. 결과적으로 XO는 다른 활성 산소종과 함께 신체의 산화 스트레스에 기여하고 염증, 죽상경화증, 암, 노화 등과 같은 많은 병리학적 과정에 관여하는 과산화물 라디칼의 중요한 생물학적 공급원으로 간주됩니다.32. 고요산혈증 치료에 대한 최근의 치료법은 XO 효소를 억제하는 것입니다. XO 억제제(알로푸리놀, 페북소스타트)를 함유한 다양한 약물이 개발되었으며, 이 약물의 사용은 불행하게도 특정 부작용과 관련이 있습니다. 이러한 이유로 이러한 합성 화합물에 대한 대안을 제공할 수 있는 천연 XO 억제제에 대한 지속적인 연구가 이루어지고 있습니다. 여러 종의 능력에 대해 문헌에 보고된 바가 있습니다. 샐비어 (S. plebeia, S. miltiorrhiza, S. verbenaca) XO를 억제하기 위해33,34,35따라서 이 활동의 발생 가능성도 연구 대상에서 테스트되었습니다. S. 프루티코사 추출물. 또한 카페산, 카르노식산, 카르노솔, 살비아놀산 B, 스쿠텔라린, 로즈마린산 및 참고로 XO 억제제 알로푸리놀과 같은 세이지에 전형적인 선택된 페놀성 화합물에서도 XO 억제 활성이 확인되었습니다.
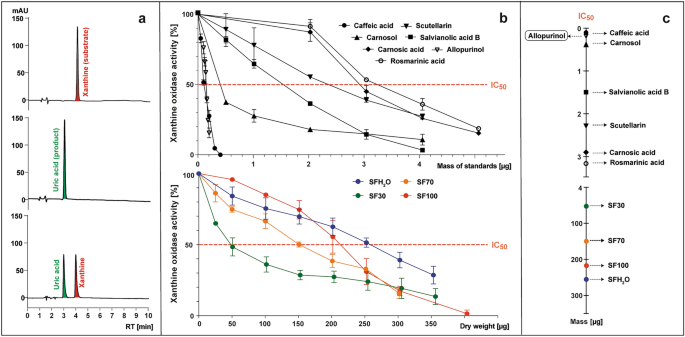
테스트 샘플의 유무에 관계없이 XO에 의한 크산틴(기질)의 요산(생성물)으로의 변환은 285 nm에서 HPLC-PAD를 사용하여 모니터링되었습니다(그림 1). 3ㅏ). 효소 활성은 샘플을 첨가하지 않은 대조군과 비교하여 테스트 샘플이 있을 때 형성된 요산 피크 면적의 백분율로 계산되었습니다(그림 2). 3비). XO 효소의 억제는 IC로 표현되었습니다.50 값은 효소 활성을 50%로 감소시킬 수 있는 샘플의 표준 또는 건조 중량(μg)의 질량을 의미합니다(그림 1). 3기원전).
다음을 포함하는 반응 후 혼합물의 285 nm에서의 HPLC 크로마토그램의 예(위부터): 크산틴; 잔틴 및 잔틴 산화효소(XO); 크산틴, XO 및 억제제(ㅏ), 이는 테스트된 표준물질(카페산, 스쿠텔라린, 살비아놀산 B, 로즈마린산, 카르노식산, 카르노솔 및 알로푸리놀) 존재 하에서 XO 활성 곡선을 나타내는 플롯을 준비하기 위한 기초가 되었습니다. S. 프루티코사 추출물(SFH2O-물 추출물; SF30-30% 에탄올 추출물; SF70-70% 에탄올 추출물; SF100 – 에탄올 추출물) (비), 이는 매개변수 IC를 결정하는 데 사용되었습니다.50, 이는 XO 활성을 50%로 감소시키는 데 필요한 테스트 샘플의 마이크로그램을 의미합니다(씨).
알려진 XO 억제제 알로푸리놀(allopurinol)이 IC와 함께 기준으로 사용되었습니다.50 0.15μg(5.5μM)의 값입니다. 연구된 모든 표준은 IC에서 XO 억제 활성을 보여주었습니다.50 범위는 0.1~3.15μg(2.8~43.8μM)입니다. XO 저해 활성은 로즈마린산 < 카르노산 < 스쿠텔라린 < 살비아놀산 B < 카르노솔 < 카페산 순으로 증가했습니다. 카페인산은 가장 낮은 IC을 보였다50 값(0.1μg; 2.8μM)은 테스트된 화합물 중에서 가장 강력한 XO 억제 활성을 나타냅니다. 이는 Wan et al.이 제시한 데이터와 일치하지 않는 알로푸리놀보다 훨씬 강력했습니다.36 그리고 Flemmig et al.37, 여기서 IC50 카페인산의 함량은 알로푸리놀에 비해 각각 거의 8~2배 낮았습니다. 이러한 차이는 테스트를 위해 선택된 XO의 출처로 인해 발생할 수 있습니다. 인용된 연구에서는 소 우유의 산화효소가 사용된 반면, 본 연구에서는 미생물 산화효소가 선택되었습니다. 이 연구에서 로즈마린산은 XO 억제 효과가 가장 낮았으나(3.2μg; 43.8μM), Ghallab et al.38 알로푸리놀과 로즈마린산의 시너지 조합으로 필요한 합성 약물의 복용량을 낮출 수 있다고 보고했습니다. XO는 연구된 모든 물질에 의해 억제되었습니다. S. 프루티코사 다른 추출물에 대해 보고된 데이터와 일치하여 알로푸리놀보다 효과가 1000배 이상 낮지만 추출물입니다. 샐비어 종. 스쿠텔라린 및 기타 플라본은 이전에 XO의 강력한 억제제로 설명되었습니다.39. SF30과 SF70 추출물 사이의 총 플라보노이드 함량에는 약간의 차이가 있었고, SF70 추출물에 더 유리한 다른 항염증 화합물 함량에도 불구하고 SF30은 XO 활성을 억제하는 가장 강력한 능력을 가졌습니다. IC50 SF30의 값은 50μg이었고 이 매개변수를 기반으로 SF70, SF100 및 SFH의 잠재적인 항염증 활성을 나타냅니다.2O 추출물은 각각 3배, 4배, 5배 약한 것으로 확인되었습니다.